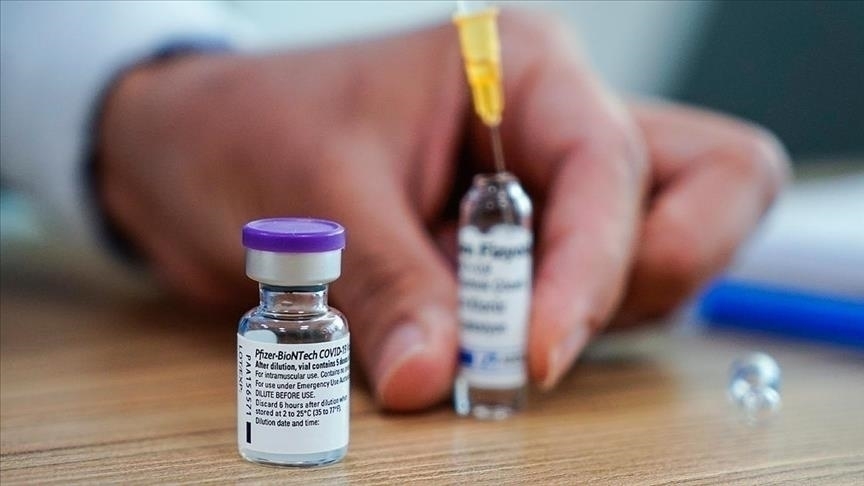
Dünya Sağlık Örgütü (DSÖ) verilerine göre, 2 Ekim itibarıyla dünya genelinde 42 COVID-19 aşı adayı, klinik denemelerle insanlar üzerinde test edilirken, 151 aşı adayı da klinik öncesi geliştirme aşamasında bulunuyor. Klinik deneme aşamasına geçen aşılardan 18’i birinci, 14’ü ikinci, 10’u ise üçüncü aşamada insanlar üzerinde test ediliyor.
Türkiye’nin 3 aşı adayı insan üzerinde denenecek
Türkiye’den klinik öncesi geliştirme aşamasında 13 aşı adayı bulunuyor.
Ege Üniversitesi, Selçuk Üniversitesi, Erciyes Üniversitesi, Mehmet Ali Aydınlar Üniversitesi, Acıbadem Labmed Sağlık Hizmetleri AŞ, Ankara Üniversitesi, İzmir Biyotıp ve Genom Merkezi, Boğaziçi Üniversitesi, Bezmialem Vakıf Üniversitesi, Ortadoğu Teknik Üniversitesi ve Koçak Farma, COVID-19 aşısı için çalışmaları yürütüyor.
Sağlık Bakanı Fahrettin Koca, 3 Ekim’de yaptığı açıklamada, bu aşılardan 3’ünün klinik deneme aşamasına geldiği duyurdu.
Bakan Koca, Erciyes Üniversitesince geliştirilen 2 aşı adayıyla Koçak Farma şirketinin Bakanlığın desteğiyle geliştirdiği aşı adayının, hayvanlar üzerinde yapılan testlerde başarı sağladığı ve böylece klinik öncesi çalışmaları tamamladığını aktardı.
Söz konusu aşı adaylarının kısa sürede insanlar üzerinde test edilmeye başlanacağını ifade eden Koca, Ankara Üniversitesinin geliştirdiği aşı adayının da klinik denemeleri için Sağlık Bakanlığına ve Türkiye Sağlık Enstitüleri Başkanlığına (TÜSEB) müracaatlarda bulunduğu, Selçuk Üniversitesince geliştirilen bir başka aşı adayının da klinik denemelere başlamaya yakın olduğunu söyledi.
Potansiyel aşılar deneniyor
Sağlık Bakanı Koca, 17 Eylül’de yaptığı açıklamada, Çinli Sinovac firmasının geliştirdiği aşı adayı “Coronavac”ın Hacettepe Üniversitesinde görevli 3 gönüllü sağlık çalışanı üzerinde test edilmeye başlandığını duyurdu.
Coronavac, “Türkiye’de insanlar üzerinde denenen ilk potansiyel COVID-19 aşısı” oldu.
Koca, ABD’li ilaç şirketi Pfizer’in BioNTech ile geliştirdiği aşı adayının 3’üncü aşama denemelerine izin verildiğini, Rusya’nın aşı adayı için yaptığı müracaatın da değerlendirildiğini söyledi.
Çin menşeili aşının ilk başta 1200 sağlık çalışanı üzerinde deneneceğini vurgulayan Koca, devamında denek sayısının 12-13 bine çıkarılmasının planlandığı bilgisini paylaştı.
CoronaVac, Hacettepe’nin ardından Kocaeli, İstanbul-Cerrahpaşa, Uludağ üniversiteleri ile Ankara Şehir Hastanesinde denenmeye başlandı.
Klinik öncesi safhayı tamamlayıp insanlar üzerinde test edilmeye hazırlanan “yerli aşılar” için de yurt içinde imalat hazırlıkları sürdürülüyor.
Dünya aşı için seferber oldu
COVID-19 salgını, tüm dünyayı etkisi altına alırken, salgından çıkışın anahtarı olarak görülen aşı geliştirme çalışmaları aynı anda birçok ülkede birden yürütülüyor.
Devlet kurumları, araştırma kuruluşları, biyoteknoloji ve ilaç şirketleri, COVID-19’a karşı bağışıklık sağlayacak aşı geliştirmek üzere seferber olmuş durumda.
Devletler ve uluslararası kuruluşlar, aşı çalışmalarına daha önce görülmemiş miktarlarda mali kaynak sağlarken, şirketler de henüz klinik deneme aşamasındaki aşılardan yüz milyonlarca doz üreterek büyük riskler alıyor.
Olağan koşullarda, bir aşının geliştirilebilmesi için 10-15 yıl kadar süren uzun bir çalışma gerekirken, COVID-19’a karşı aşı geliştirme çalışmalarında bu kadar hızlı mesafe kat edilmesinde dünya çapında etkisini gösteren salgının yarattığı aciliyetin yanı sıra DNA teknolojisindeki ilerlemelerin etkisi oldu.
Klinik denemelere başlayan potansiyel aşılar
Çin’in 11 Ocak’ta COVID-19’un DNA dizilimini açıklamasının ardından dünyanın pek çok ülkesindeki araştırmacılar, genetik kopyasını ürettikleri virüs üzerinde laboratuvarlarda çalışmaya başladı.
Virüsün genetik diziliminin bilinmesi, aşı geliştirme sürecinin hazırlık safhasını hızlandırarak klinik denemelere çabuk geçilebilmesinin yolunu açtı.
COVID-19’un genetik yapısının 2002-2003’te Çin’den dünyaya yayılan Şiddetli Akut Solunum Yolu Sendromu’na (SARS) yol açan koronavirüsle büyük ölçüde örtüşmesi, araştırmacılara SARS’a karşı aşı bulmak için yapılan geçmiş çalışmalardan yararlanma imkanı sağladı.
Binlerce deneğin katıldığı, 3’üncü aşama klinik denemelere başlayan potansiyel aşılar arasında ABD’den 3 ve Avrupa’dan 2, Rusya’dan 1 ve Çin’den 4 aday yer alıyor.
Moderna ve “mRNA-1273”
ABD’de “Moderna” ilaç firmasının Ulusal Alerji ve Bulaşıcı Hastalıklar Enstitüsü (NIAID) iş birliğiyle geliştirdiği aşı adayı “mRNA-1273” için 27 Temmuz’da 3’üncü aşama klinik denemelerin başladığı duyuruldu.
Merkezi Boston kentinde bulunan “Moderna”, Çin’in COVID-19’un genetik dizilimini açıklamasından yalnızca 2 gün sonra potansiyel bir aşı geliştirdiğini belirtti.
Ribo Nükleik Asit (RNA) temelli aşı, virüsün insan hücresine tutunmasını sağlayan “çivi proteini” adı verilen enzimi baskılayarak, vücutta bağışıklık sağlamayı hedefliyor.
ABD Gıda ve İlaç İdaresinin (FDA) onay vermesinin ardından aşının 1’inci aşama klinik denemeleri, 17 Mart’ta Washington eyaletinde başlarken, mRNA-1273, “insanlar üzerinde denenmeye başlanan ilk potansiyel COVID-19 aşısı” oldu.
Aşı adayının klinik denemelerinin 3’üncü aşamasında 30 bin kişi üzerinde test edilmesi planlanıyor.
Halen ABD’de 38 merkezde sürdürülen denemelerden, 2020 sonu veya 2021 başlarında sonuç alınması umuluyor.
Oxford ve “AZD1222”
İngiltere’de Oxford Üniversitesi Jenner Enstitüsü ile Oxford Aşı Grubu iş birliğinde geliştirilen ve üretim lisansı İngiliz-İsveç ilaç şirketi AstraZeneca tarafından satın alınan aşı adayı “AZD1222” için İngiltere ve Hindistan’da 2’nci ve 3’üncü aşama, Brezilya, Güney Afrika ve ABD’de 3’üncü aşama klinik denemeler yürütülüyor.
Aşı adayı, insanlarda basit soğuk algınlığına yol açan bir adenovirüsün zayıflatılmış ve kendini çoğaltamayan bir versiyonunu içeriyor. Aşı adayı, COVID-19’un insan hücrelerine tutunmasını sağlayan çivi proteininin yapay şekilde ortaya çıkmasını ve vücudun buna karşı koruyucu antikorlar üreterek gerçek virüse bağışıklık kazanmasını amaçlıyor.
Dünya çapında 30 bin sağlıklı gönüllü üzerinde test edilmesi hedeflenen aşı adayı için ABD 1,2 milyar dolar kaynak sağlarken, Avrupa Birliği (AB) ülkeleri testlerin başarılı olması halinde şirketten 400 milyon doz aşı satın alma konusunda anlaştı.
Hindistan Serum Enstitüsü (SII) iş birliğiyle denemelerde kullanılmak üzere milyonlarca doz aşı üreten şirket, aşı adayının ekim sonunda acil kullanıma hazır hale getirilmesini hedefliyor.
BioNTech ve “BNT162b1”
Almanya’da Türk bilim insanı Prof. Dr. Uğur Şahin’in kurucu ortağı olduğu biyoteknoloji firması BioNTech’in geliştirdiği “BNT162b1” adlı aşı adayı da 3’üncü aşama denemelere geçen aşı adayları arasında yer aldı.
4 ayrı formül olarak geliştirilen aşı adayının “b1” ve “b2” versiyonları, insanlar üzerinde test edilmeye başlandı.
RNA temelli aşı, COVID-19’u etkisiz kılan kan şekeri enzimleri ile alımlayıcı-bağlayıcı İmmünoglobulin G antikorlarını harekete geçirmeyi, hücre düzeyinde bağışıklık tepkisi yaratan CD4+ ve CD8+ glikoproteinleri artırmayı amaçlıyor.
Katılımcı sayısını artırmak için başvuru
ABD’de Pfizer, Çin’de Fosun Pharma ilaç firmalarının üretim lisansını aldığı aşı adayı için 1. ve 2. aşama klinik denemelerinin Almanya’da yürütülmesinin ardından 27 Temmuz’da ABD ile Arjantin ve Almanya’nın aralarında olduğu diğer ülkelerde 30 bin sağlıklı gönüllünün katılması hedefiyle 3. aşama klinik denemeler başlatıldı.
Pfizer, 12 Eylül’de denemenin katılımcı sayısını 44 bine çıkarmak için ABD Gıda ve İlaç İdaresine (FDA) başvuruda bulundu.
Şirket Üst Yöneticisi Albert Bourla, 14 Eylül’de, aşının etkinliğine dair kesin sonuçları ekim sonuna kadar almayı beklediklerini, tescil, imalat ve dağıtım süreçleri için de hazırlıklara başladıklarını söyledi.
ABD yönetimi, testlerin başarılı olması durumunda aralıkta 100 milyon doz, sonrasında 500 milyon doz daha aşı satın almak üzere Pfizer ile 1,9 milyar dolarlık anlaşma yaptı.
Japonya aşıdan 120 milyon doz, AB ise 200 milyon doz satın almak üzere anlaşmaya vardı.
Çin’deki çalışmalar
COVID-19’un ortaya çıktığı Çin’de de 11 aşı adayının klinik denemeleri sürüyor. Bunlardan 4’ü birinci, 2’si ikinci, 5’i ise üçüncü aşamada insanlar üzerinde test ediliyor.
Sinopharm, Sinovac ve CanSino gibi kamuya ait ilaç firmaları, Çin Askeri Tıp Akademisi, Vuhan Viroloji Enstitüsü, Pekin Biyolojik Ürünler Enstitüsü gibi kurumlarla iş birliği içinde aşı çalışmaları yürütüyor.
SinoVac’ın geliştirdiği “CoronaVac”, Sinopharm’ın Vuhan Viroloji Enstitüsü ve Pekin Biyolojik Ürünler Enstitüsü ile geliştirdiği 2 aşı adayı ile CanSino’nun Çin Askeri Tıp Akademisi ile iş birliğinde geliştirdiği “Ad5-NCov” adlı aşı adayı, en fazla umut bağlanan çalışmalar arasında görülüyor.
Sinopharm
Sinopharm’ın ürettiği isimsiz iki aşı adayı, formüllerinde COVID-19’un “etkisizleştirilmiş” bir hali olan virüs bileşeni bulunduruyor.
Aşı adayları, vücudun güçsüzleştirilmiş virüse karşı doğal korumalarını canlandırmayı, bu yolla bağışıklık tepkisi yaratmayı amaçlıyor.
1. ve 2. aşama klinik denemeleri Çin’de yürütülen aşı adaylarının, 3. aşama klinik denemeleri 17 Temmuz’da Birleşik Arap Emirlikleri’nin (BAE) başkenti Abu Dabi’de başladı.
45 bin sağlıklı gönüllünün katılması planlanan denemeler, ilave olarak Bahreyn ve Ürdün’de sürdürülüyor.
SinoVac ve “CoronaVac”
Çinli ilaç şirketi Sinovac’ın geliştirdiği CoronaVac da 3’üncü aşama klinik denemelere başlayan aşı adayları arasında bulunuyor.
Çin hükümeti, 1. ve 2. aşama denemelerde etkinliği kanıtlanan ve ciddi bir yan etkiye rastlanmayan aşı adayının acil durum kullanımına izin verdi.
Formülünde virüsün etkisizleştirilmiş bir versiyonunu içeren aşı adayı için 21 Temmuz’da Brezilya’da, 11 Ağustos’ta Endonezya’da 3. aşama klinik denemelere başlandı.
Brezilya’daki denemede 8 bin 870, Endonezya’daki denmede ise 1620 sağlıklı gönüllünün aşılanması planlanıyor.
3. aşama denemeler kapsamında 17 Eylül’de insanlar üzerinde test edilmeye başlanan Coronavac, “Türkiye’de denen ilk COVID-19 aşısı” oldu.
CanSino ve “Ad5-NCov”
CanSino’nun Çin Askeri Tıp Akademisi ile iş birliğinde geliştirdiği “Ad5-NCov” da 3’üncü aşama denemelere başlanan aşı adayları arasında yer aldı.
Soğuk algınlığına yol açan zararsız bir adenovirüsle insan vücuduna COVID-19’un genetik bileşenlerini aktararak bağışıklık tepkilerini uyandırmayı hedefleyen Ad5-nCOV’un güvenliğinin ve bağışıklık etkisinin test edildiği 1. ve 2. aşama klinik denemeleri, Çin’de yürütüldü.
Aşı adayının 3. aşama denemeleri 9 Ağustos’ta Suudi Arabistan’da başladı. 19 Ağustos’ta Pakistan, 3 Eylül’de Rusya, aşı adayının klinik denemelerine onay verdi.
Toplam 40 bin kişinin katılması planlanan klinik denemelerin, Brezilya ve Şili’de de yürütülmesi planlanıyor.
Çin ordusu, 25 Haziran’da aşı adayının “özel ihtiyaç sağlık malzemesi” olarak kullanımını onayladı.
Rusya ve “Sputnik V” aşısı
COVID-19 için aşı geliştirilen ülkelerden biri de Rusya oldu.
Gamaleya Ulusal Epidemioloji ve Mikrobiyoloji Enstitüsünün geliştirdiği “Sputnik V” adlı COVID-19 aşı adayı, kısa süren 1. ve 2. aşama klinik denemelerin ardından 3. aşamada insanlar üzerinde test edilmeye başlandı.
Aşı adayı, Oxford aşısı gibi soğuk algınlığına yol açan bir adenovirüsten alınan, kendini çoğaltamayan, ayrı dozlar halinde uygulanan iki virüs bileşeni (rAd26 ve rAd5) içeriyor.
Rusya Devlet Başkanı Vladimir Putin, 11 Ağustos’ta yaptığı açıklamada, aşı adayının erken aşamadaki klinik denemelerde kaydettiği olumlu sonuçların ardından “aşı” olarak tescillendiğini ve yaygın kullanımına başlanacağını duyurdu.
Ancak DSÖ yetkilileri, Rusya’nın iddiası karşısında temkinli bir tutum izlenmesini salık verdi.
Yetkililer, bir aşı adayının yaygın kullanım için tescillenebilmesi için klinik denemelerinin eksiksiz tamamlamış olması gerektiğini vurgulayarak, prosedürlerin aceleye getirilmesinin halk sağlığı bakımından sakıncaları olacağına dikkati çekti.
Ülke genelinde yaygın bir gönüllü aşı kampanyası yürütmeyi hedefleyen Rusya, aşı tedariki için Brezilya, Meksika ve Hindistan ile anlaşmalara vardı.
Janssen ve “Ad26COVS1”
Amerikan ilaç devi Johnson & Johnson’ın bağlı iştiraki Belçikalı Janssen ilaç şirketi de aşı adayı “Ad26COVS1” için 15 Temmuz’da Belçika ve ABD’de başladığı klinik denemeleri 3. aşamaya taşıdı.
“Adenovirüs serotip 26” adı verilen tekil bir virüs bileşeni içeren aşı adayı, COVID-19’un insan hücrelerine tutunmasını sağlayan “çivi proteine” istikrarlı bir yapay ifade kazandırarak, vücutta virüsü körelten ve etkisizleştiren antikorları canlandırmayı amaçlıyor.
Şirket, tek doz olarak uygulanan aşı adayının 3. aşama denemelerine 23 Eylül’de başladı.
ABD, Güney Afrika, Arjantin, Brezilya, Şili, Kolombiya, Meksika, Peru, Filipinler ve Ukrayna’da yürütülmesi planlanan denemelere 60 bin gönüllünün katılması hedefleniyor.
ABD hükümeti, şirketle aşı adayının başarılı olması halinde, ilk etapta 100 milyon sonrasında 200 milyon doz satın almak üzere 5 Ağustos’ta anlaşmaya varmıştı.
Novavax ve “NVX-CoV2373”
ABD’li ilaç firması Novavax’ın aşı adayı “NVX-CoV2373” de 3. aşama denemelere başlayan potansiyel COVID-19 aşıları arasında yer alıyor.
Şirket, aşı adayının 3. aşama klinik denemelerine 24 Eylül’de İngiltere’de başladı.
İngiliz hükümetinin Aşı Görev Gücü iş birliğinde yürütülen denemeye 18 ile 84 yaşları arasındaki 10 bin gönüllünün katılması hedefleniyor.
Genetik mühendisliğiyle üretilmiş COVID-19 glikoprotein partikülünü içeren aşı adayı, şirketin diğer aşılarında kullandığı güçlendirici katkı maddesiyle (adjuvan) daha fazla antikor ve daha uzun süreli bağışıklık üreterek, bağışıklık tepkisini artırmayı amaçlıyor.
ABD hükümeti, Maryland eyaletinde faaliyet gösteren şirkete, gelecek yılın başında 100 milyon doz COVID-19 aşısı üretmesi halinde 1,6 milyar dolar ödemeyi taahhüt etmişti.
Anılan ülkeler dışında Hindistan, Japonya, Güney Kore, Tayvan, Singapur, Kanada, Avustralya, Fransa, İtalya, Kazakistan ve Küba’da da COVID-19 aşı adaylarının klinik denemeleri yürütülüyor.
Aşı ne zaman hazır olacak?
Tüm bu çalışmaların ne zaman sonuçlanıp, yaygın olarak kullanılabilecek bir aşının ortaya çıkacağı ise belirsizliğini koruyor.
Klinik denemelerde başarı kaydedilmesi halinde aşıların gelecek aydan itibaren yaygın kullanımına başlanabileceği ifade edilirken; ABD, Rusya ve Çin gibi ülkeler buna ilişkin hazırlıklar yapıyor.
Uluslararası sağlık kurumları ise aşıların geliştirilmesinin aceleye getirilmemesi gerektiği uyarısında bulunuyor.
Çok yönlü biyolojik etkileri olan ve zaman içinde mutasyon geçirebilen virüslere karşı standart bir aşı üretmek her zaman mümkün olmuyor.
Örneğin; COVID-19’un öncülü olan SARS koronavirüsünün ortaya çıkmasından bu yana 20 yıla yakın zaman geçmesine karşın aşı geliştirilemedi. 1980’li yıllarda AIDS’e yol açan HIV virüsüne karşı başlatılan aşı geliştirme çalışmaları da sonuçsuz kaldı.
Hangi aşamada insanlar üstünde deneniyor?
Bir aşının yaygın olarak kullanılabilmesi için 3 aşamada insanlar üzerinde test edilmesi gerekiyor.
Klinik denemelerin ilk aşamasında, az sayıdaki gönüllü sağlıklı denek üzerinde aşının güvenli olup olmadığı ve insanlar üzerindeki muhtemel yan etkileri araştırılıyor.
İkinci aşamada, aşının bağışık tepkilerini uyandırmadaki etkinliği 100’den fazla denek üzerinde test ediliyor.
Üçüncü ve son aşamada ise aynı işlem, binlerce denekle tekrarlanıyor. Tüm bu süreç, aylar ve hatta yıllar alabiliyor.
Çin’in Vuhan kentinde Aralık 2019’da ortaya çıkan COVID-19, 200’den fazla ülke ve bölgeye yayılarak salgına dönüştü. Dünya genelinde vaka sayısı 36 milyon 400 bini aşarken 1 milyon 60 binden fazla kişi hayatını kaybetti.
TRT